世界最小のコイル状バネを設計し、細胞への“微小な力”の計測に成功
〜生物の力学情報処理メカニズムの解明に期待〜
2023年7月3日
ポイント
-
DNAを材料にして世界最小のコイル状バネを設計し、細胞への“微小な力”の超高感度計測に成功
-
この計測技術により、生物の機械的な情報処理のメカニズムを解明するための研究が大きく前進
-
今後、超省エネの情報処理システムを実現し、新しい原理のコンピュータの開発等につながることに期待
国立研究開発法人情報通信研究機構(NICT、理事長: 徳田 英幸)の岩城光宏主任研究員らの研究グループは、国立研究開発法人理化学研究所(理研、理事長: 五神 真)と共同で、DNAを材料に世界最小のコイル状バネを設計し、細胞への“微小な力”の超高感度計測に成功しました。
まだ詳細が分かっていない「脳や細胞における超省エネの機械的な力の情報処理メカニズム」を解明することができれば、全く新しい原理によるコンピュータの開発等につながることが期待されています。
今回開発したのは、細胞へのノイズレベルの“微小な力”の大きさと向きを、サブピコニュートン精度で検出する“世界初”の計測技術です。この計測技術によって生物の力学情報処理メカニズムを解明するための研究が大きく前進し、今後、超省エネで電力消費の少ない全く新しい原理の情報処理システムを実現する新たな指針を得ることが期待されます。
なお、本成果は、2023年7月3日(月)10:00(日本時間)に、米国科学雑誌「ACS Nano」に掲載されました。
背景
生物は、コンピュータよりも極めて少ない消費エネルギーで複雑な情報処理を行っており、神経伝達物質のような化学分子や電気で互いに情報のやり取りをしていることはよく知られています。
近年、機械的な力を信号として情報のやり取りを行っていることが分かってきました。ノイズレベルの“微小な力”も高感度に検出して力学情報処理しているため、超省エネな情報処理に寄与していると考えられていますが、そのメカニズムは分かっていません。
その一因として、細胞が検知している“微小な力”を高感度で計測する技術が大きく不足していることが挙げられますが、既存の計測技術では、「“微小な力”の時間的な変動を正確にとらえることができない」「力の測定レンジが狭い」「力の大きさと同時に向きの情報を高い時間分解能で得ることができない」などの問題を抱えていました。
今回の成果

図1 DNAを材料に設計したタンパク質サイズの世界最小のコイル状バネの模式図
様々な分子に連結可能で、バネの硬さもプログラムすることができる。
今回の研究では、DNAを材料にしてタンパク質サイズの世界最小のコイル状バネ(ナノスプリング)を設計し(図1参照)、細胞とガラス基板の間に連結させて(図2参照)、細胞への“微小な力学情報(大きさと向き)”をサブピコニュートン精度で精密計測することに世界で初めて成功しました。
直径35ナノメートル、長さ200〜700ナノメートルのナノスプリングを設計し、その一端を細胞膜表面に存在するインテグリンに連結し、もう一端には細胞外部のガラス基板に連結しました。両者の間で力学的な情報のやり取りが起こると、ナノスプリングが伸展もしくは短縮するのが観察され、伸展の向きの変化も同時に観察することができました。さらに、これらの変化をナノメートル精度で精密に画像解析する手法も新たに開発することで、力の大きさと向きの時間的な変動を同時に計測することができました(図2参照)。ナノメートル解像度での計測を実現したことで、ノイズレベルの“微小な力” (〜1ピコニュートン)も含めた動的な変動を容易に検出することが可能になりました。
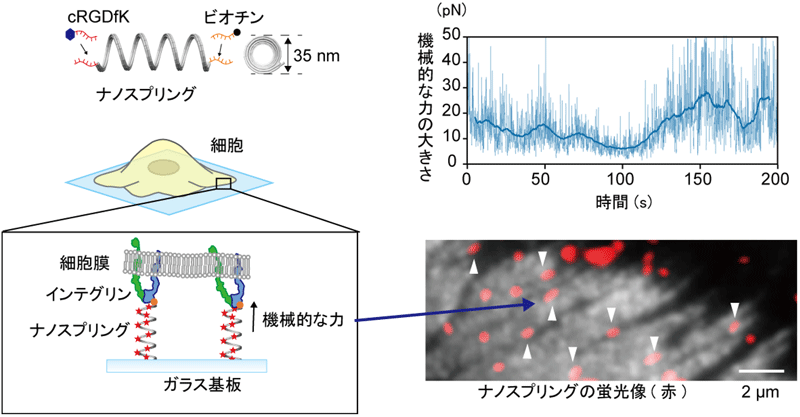
図2 ナノスプリングを用いた細胞の検知する機械的な力の計測例
ナノスプリングの両末端を1本鎖DNAとし、これらと相補的な配列を持つ1本鎖DNAを介して、インテグリン結合分子(RGDペプチド, cRGDfK)及びガラス基盤への接着分子(ビオチン)をナノスプリングにつなげた。これにより、インテグリンとガラス基板の間をナノスプリングで連結し、蛍光観察によって伸展長を精密計測することで、ピコニュートンの“微小な力”の変動が世界で初めて検出できた。(白矢印のバネが伸展している。)
今後の展望
細胞内部では、様々な接着斑形成分子やアクトミオシンなどが動的に揺らいで自己集合と離散を繰り返しながら、インテグリンを介した“微小な力学信号”を検出・情報処理し、細胞運動や遺伝子発現の調整などを行っていることが分かっています。このように、システムが内包する“ゆらぎ(ノイズ)”を利用しながら情報処理する仕組みは、既存のコンピュータとは全く異なる原理であり、生物の超省エネな情報処理を実現するための重要な特徴であると考えられています。
一方で、既存のコンピュータは、ノイズを抑制してシステムを制御するため、情報処理に大きな消費エネルギーを必要とします。近年の情報処理量の増大やシステムの複雑化を受けて、必要な電力量は莫大となっていくため、その対応が喫緊の課題の一つとなっています。今回の技術開発を通して生物の力学情報処理の仕組みを学ぶことで、超省エネで電力消費の少ないノイズロバストな情報処理システムを実現する新たな指針を得ることが期待されます。
各機関の役割分担
-
情報通信研究機構: ナノスプリングの設計、音響力顕微鏡でのバネ特性の評価、実験データの解析、画像解析プログラム開発
- 理化学研究所: 細胞実験とナノスプリング蛍光観察の実施、実験データの解析
論文情報
掲載誌: ACS Nano
DOI: 10.1021/acsnano.2c12545
論文名: A programmable DNA origami nanospring that reports dynamics of single integrin motion, force magnitude and force orientation in living cells
著者: 松原瞳、福永裕樹、齊藤崇啓、池崎圭吾、岩城光宏
なお、本研究の一部は、国立研究開発法人日本医療研究開発機構(AMED)革新的先端研究開発支援事業「メカノバイオロジー機構の解明による革新的医療機器及び医療技術の創出」の一環として、JP20gm5810022の助成、及び科学技術振興機構(JST)戦略的創造研究推進事業(CREST)「多細胞間での時空間的相互作用の理解を目指した定量的解析基盤の創出」の一環として、JPMJCR2023の助成を受けて行われました。
補足資料
DNAを材料に設計したナノスプリングに関する資料
1. ナノスプリングの設計原理と設計例
ナノスプリング開発の基礎となるDNAオリガミは、2006年にポール・ラザマンドによって提唱された技術です。DNAは、A,T,G,Cの4種類の核酸塩基が相補的に対を成し右巻きの二重らせん構造を取りますが、DNAオリガミでは、DNA二重らせんを束ねることで任意のナノ構造物が形成されます。7,000〜8,000塩基から成る長鎖1本鎖 DNA(スカフォールドDNA)に対して、100種類以上の短い(30〜50塩基)オリゴDNA(スカフォールドの相補配列を持つ)がスカフォールドDNAに結合し、折り畳んでいきます(図3(a)参照)。オリゴDNAがスカフォールドDNAを折り畳んで固定するホッチキスの役割を果たすことから、これらのオリゴDNAをステープルDNAと呼びます。当初は、2本鎖DNAが横並びになることで形成される平面的なシート構造の設計のみが可能でしたが、現在では、シートを更に折り畳み重ね、ステープルDNAで固定することで、3次元的なナノ構造物の設計も可能となり、立方体や直方体構造が報告されてきました。さらに、直線状のDNA二重らせんをただきれいに束ねるだけだと、平面構造とその折り畳み構造物にしかなりませんが、DNA構造を少しだけ歪ませるようにして束ねる設計をすることで、曲線から成る束を設計できる手法も報告され、ナノスプリングでは、この手法を応用して、3次元的なコイル構造形成に成功しました(図3(b)、(c)参照)。無機材料を用いてコイル形状のバネを作成する場合では、半導体の製造で用いられるリソグラフィのように、光や電子ビームを用いて材料をトップダウン的に加工することが必要であり、最小でも数百ナノメートルのコイル半径を持ちますが、ナノスプリングのコイル半径は20〜35ナノメートルであり、数十倍の微細化となります。また、コイル形状を採用することで、コイル半径、コイル線の太さ、巻き数の変更によって、バネの硬さ(バネ定数)のチューニングが容易となります。
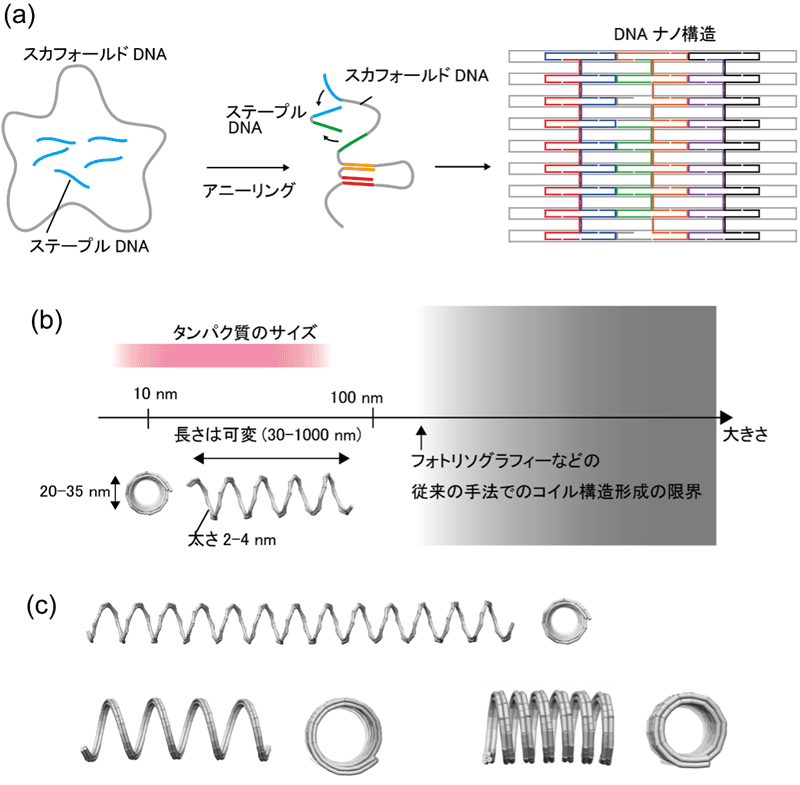
図3 ナノスプリングの設計原理と設計例
(a) DNAオリガミ技術を用いて2次元的なシート構造を作成するときの流れ(b) ナノスプリングのサイズ
(c) 硬さや長さの違う様々なナノスプリングの設計の例
2. ナノスプリングのバネ特性の評価
設計したナノスプリングがナノサイズのバネとして機能することを確認するために、音響力顕微鏡を用いてナノスプリングを1本ずつ伸展・短縮させて、バネの長さと力の大きさを評価しました。まず、ナノスプリングの一端をガラス基板に固定して、他端をシリカビーズに連結しました。ピエゾ素子を用いて超音波を発生させると、シリカビーズに音響力が掛かるので、ナノスプリングの伸展が起こります(図4(a)参照)。シリカビーズの動きからナノスプリングの長さを計算すると、音響力の大きさに応じて700ナノメートル程度までの伸展が観察されました(図4(b)参照)。ナノスプリングの長さと力の大きさの関係から、今回、設計したバネは、50ピコニュートン程度まで緩やかに伸展する特性を持つことが分かり、また、溶液の条件を変えても、その特性はほとんど変化しないことも分かりました(図4(c)参照)。これにより、ナノスプリングがナノサイズのバネとして機能し、生体内の分子レベルで発生する“微小な力”のレンジであるピコニュートンオーダーで感度良く計測できることが実証されました。
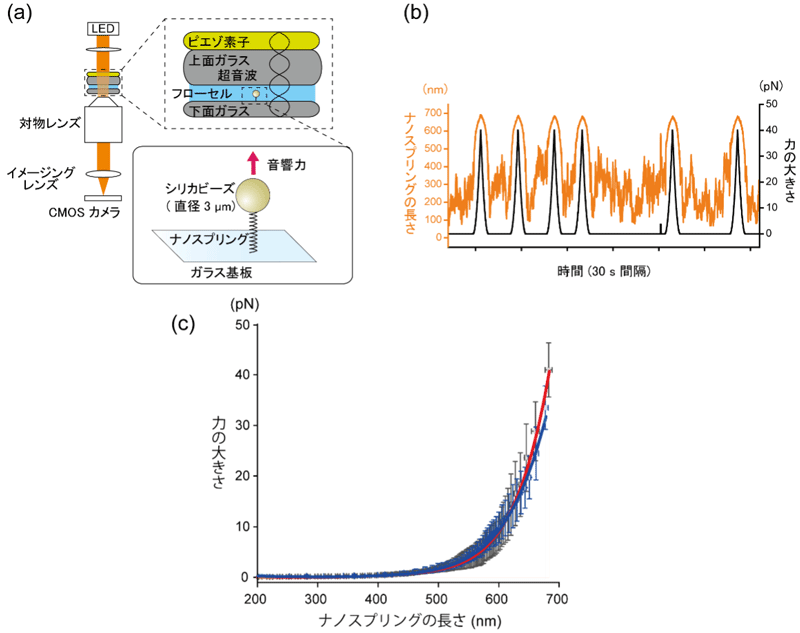
図4 ナノスプリングのバネ特性の評価
(a) 音響力顕微鏡での測定の模式図(b) ナノスプリングを伸展させる力の大きさとナノスプリングの長さの時間的な変化
(c) ナノスプリングの長さと力の大きさの関係。赤線: 細胞培養液での測定、青線: DNAの保存液として一般的なTEバッファでの測定
細胞が検知する“微小な力”の計測に関する資料
インテグリンは、細胞が外部環境の“微小な力”を検知し細胞内部に伝達する重要な役割を果たします。細胞膜外に出ているインテグリンの一部は、アルギニン-グリシン-アスパラギン酸から成るRGD配列を認識し結合するので、ナノスプリングの片端にRGDペプチド(cRGDfK)を修飾し、もう片端には、ガラス基板の底に固定するためのビオチン修飾を施すことで、インテグリンとガラス基板とを連結することにしました。また、ナノスプリングの伸展を蛍光観察するために、蛍光色素ラベルを施しました(図5(a)、(b)参照)。
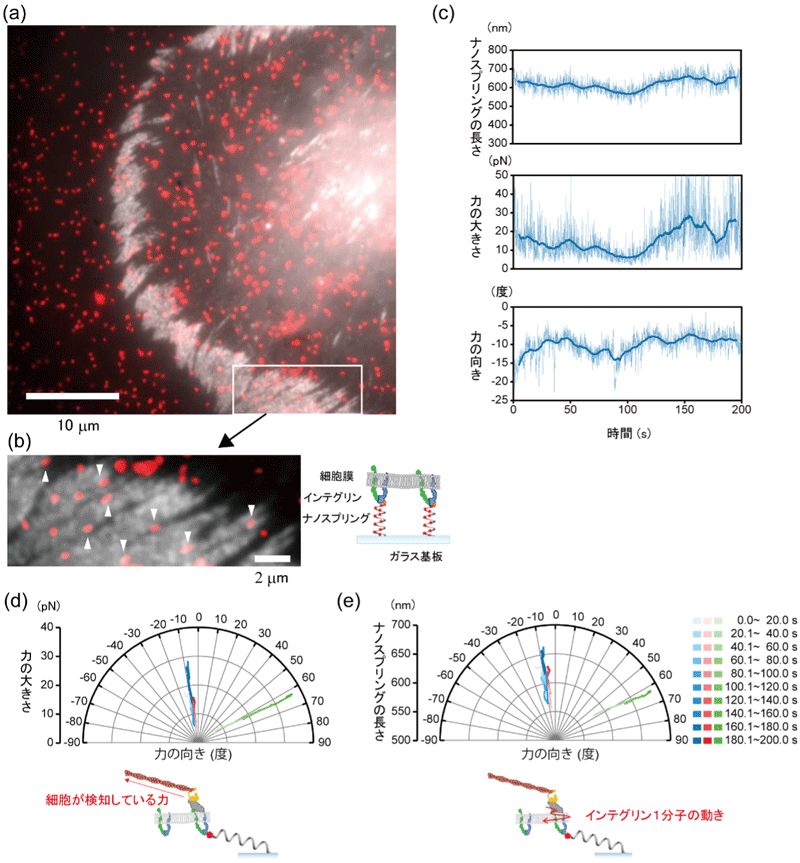
図5 細胞が検知する“微小な力”の計測
(a) 蛍光ラベルしたナノスプリング上で培養した線維芽細胞。赤: ナノスプリング、白: 細胞接着斑に集積するパキシリン(b) 図(a)の四角のエリアを拡大した像。白矢印: 伸展したナノスプリング
(c) ナノスプリングの長さ、力の大きさ及び力の向きの時間的な変動の様子
(d) 力の大きさと向きの相関図。細胞が検知している力のベクトル情報を示す。
(e) ナノスプリングの長さと力の向きの相関図。細胞膜上でのインテグリン1分子の動きを示す。
ガラス基板にナノスプリングを固定後、ヒトの皮膚組織由来の線維芽細胞を培養すると、インテグリンが集積している接着斑直下のナノスプリングが伸展しているのが観察されました(図5(b)参照)。画像解析によって、ナノスプリングの伸展長をナノメートル精度で計測し、力の変動を高感度に検出することができました。また同時に、力の向きの変動も計測することができました(図5(c)参照)。細胞が検知する力の大きさ、向き共に秒の時間スケールにて緩やかな力の上昇と降下を繰り返し(図5(d)参照)、また、細胞膜上のインテグリンも数十ナノメートル程度、前後に移動する(図5(e)参照)ことが確認できました。既存のイメージング技術である、ピラーアレイやトラクションフォース顕微鏡、もしくは、既存の分子サイズのフォースセンサのほとんどは、複数のインテグリン分子が検知する力学情報を足し合わせた結果しか計測できず、微小かつ動的な力学情報を得るのに限界がありましたが、1分子解像度での計測を実現したことで、ノイズレベルの“微小な力”(〜1ピコニュートン)も含めた動的な変動を容易に検出することが世界で初めて可能になりました。
細胞は、力学信号を内部で処理して、細胞の運動方向を制御し、遺伝子発現のパターンを変えるなど様々な細胞応答につなげています。力学信号には、信号の強度(力の大きさ)、向きだけでなく、周波数といった時間的な変動を伴う情報も含みますが、細胞がこれらの情報をどのように処理しているのか、まだほとんど分かっていません。しかも、細胞が情報処理に使えるエネルギーは、電気エネルギーが利用できる人工機械と異なりごくわずかであり、処理を行うタンパク質群が細胞内で動的に揺らいで集合・離散を繰り返しています。“微小な力学信号”の可視化と合わせて、細胞内部の情報処理の様子を分析することで、生物が持つ省エネな力学情報処理の仕組みを理解できると期待されます。
用語解説
ピコニュートン
ニュートンは力の単位であり、1ピコニュートンは1兆分の1ニュートン。
インテグリン
細胞表面に存在するタンパク質で、細胞外のコラーゲンなどに直接、結合することで力学情報を感受し、細胞内部の様々な分子に情報を伝達する役割を担う。
接着斑形成分子
細胞が周囲の物体に接着する際に、接着面において焦点接着斑とよばれるタンパク質の集合構造が形成される。この構造を形成するタンパク質分子群の総称。
アクトミオシン
力を発生するミオシンモータータンパク質と細胞骨格となるアクチンフィラメントの複合体のこと。筋細胞内では筋収縮を引き起こし、その他の細胞種でも細胞運動や接着力を発生させる。
ノイズロバスト
情報処理や機械の動作に不要となる雑音(ノイズ)の影響を受けにくいという意味。
DNAオリガミ
DNAを材料にして折り紙のように折り畳むことで、思いどおりの2次元又は3次元のナノ構造物を作り上げる技術。DNAナノテクノロジーの一種。
音響力顕微鏡
超音波を用いて微小な物体に機械的な力を加えて、物体の移動をナノメートル精度で計測するための顕微鏡。超音波を発生させる機器を制御することで、ピコニュートンオーダーの様々な大きさの力を定量的に加えることができる。
ピラーアレイ
ポリジメチルシロキサン(PDMS)を用いて作製された、直径数マイクロメーターの微細な円柱(マイクロピラー)が並んだ基板のこと。この上で細胞培養を行うと、細胞はピラーに接着、牽引するため、ピラー中心位置が移動し、その移動距離とピラーの硬さから牽引力を計算することができる。
トラクションフォース顕微鏡
直径0.2〜1マイクロメーターの蛍光ビーズを埋め込んだアクリルアミドゲル上で細胞培養を行い、蛍光観察によって得られる蛍光ビーズの動きから牽引力を計算するための顕微鏡。
本件に関する問合せ先
国立研究開発法人情報通信研究機構
未来ICT研究所 神戸フロンティア研究センター
バイオICT研究室
岩城 光宏
E-mail: iwakim nict.go.jp
nict.go.jp
 nict.go.jp
nict.go.jp広報(取材受付)
国立研究開発法人情報通信研究機構
広報部 報道室
E-mail: publicity nict.go.jp
nict.go.jp
 nict.go.jp
nict.go.jp
国立研究開発法人理化学研究所
広報室 報道担当
Tel: 050-3495-0247
E-mail: ex-press ml.riken.jp
ml.riken.jp
 ml.riken.jp
ml.riken.jp